卒中实验设计的基本原则
书号:ISBN 978-7-5046-6264-4/R · 1648
卒中实验设计的基本原则
实验设计即组织合理的实验进程确保得到正确的数据,尽可能清晰和有效的对感兴趣的问题进行解释。实验前,首先要明确实验本身要阐明的问题。我们应该尝试着去了解实验单元中各种已有或可能的来源,因为一个实验的目的之一是在回答感兴趣的问题,即我们设计实验证实自己的想法。某种意义上,研究中的实验设计比分析更重要。欠缺的研究分析可以重新分析,但是设计糟糕的实验不可能重做;实验设计的重要性同时体现在它决定如何分析数据。实验设计包含动物或样品的随机性,重复性以及双盲实验中偏差可控性。
(1)随机性
随机实验是用于检测试剂、仪器或步骤有效性的一种方法。它被认为是最可信的科学依据,因为它可以控制那些轻易改变医学研究有效性的主要偏差。
2)完全随机性
3)随机置换区域
(2)重复性
重复性即重复整个研究,与其相关的各种变化都可以预计。重复性和反复测量是不同的,重复性不应与反复测量相混淆,后者是指在一项研究中对某一现象进行反复测量。重复性遵循的是科学方法,某一实验可以被精确重复。
由某研究人员或研究小组进行的实验结果,一般是由其他独立体系的研究人员通过重复原始实验进行评价。基于原有实验描述的基础上,他们自己重复相同实验,并确定该实验结果是否与原始实验组所报道的一致。不能被准确复制的实验,一般认为不能提供有用的科学证据。结果高度重复的研究者相对于结果很难重复者将获得更多的信任。
(3)样本大小
重复性也同样与每个研究中样本大小相关。如果在一个研究中,实验组的规模太小,这项研究将无法回答所提出的问题,是对时间和金钱的浪费。然而,在较小规模就足够的情况下,研究中实验组的规模太大,是对动物和其他资源的浪费。正确估计样本规模,以确保结果是一个研究设计的重要组成部分。各组的大小应足以让有意义的原始数据被科学解释。因此,动物或独立群体的准备数量应足以证明或排除所测试生物的特质,同时应该考虑到样本大小和生物效应变化,实验设计中应该包括适当的阳性和阴性对照组。
适当的样本大小取决于四个关键因素;I型和Ⅱ型错误率α、β,数据的σ²变异性。效果大小d。在一个测试中,效果大小是我们所期望的两个不同的处理组或者是临床上有意义的差异。
通常情况下,α、β分别固定在5%和20%(或10%)。2组连续结果平行测试中,每组所需的样本大小,简单的公式是n=16σ²/d²,其两边α、β分别固定在5%和20%。例如,在减少卒中大鼠梗死体积测试中,如一梗死体积为40立方毫米(即处理和未处理的梗死面积差额为40立方毫米),并与学科标准差为35立方毫米,研究中每组所需大鼠样品为N:
N=16×35²/40²=16×1225/1600=12
(4)可疑测定值的取舍
误差是客观存在的,因此平行测定的数据总是参差不齐,有时会出现一两个与其结果相差较大的测定值(称为可疑值或异常值),可疑值要不要呢?如果已经证明是由于过失误差造成的,应该舍去。如果原因不明,就必须按照一定的统计方法进行检验,再做出取舍的判断。
①计算Q值
Q值越大,x疑离群越远,远到一定程度就舍弃。
②查Qp,n:若Q计>Qp,n,则以一定的置信度弃去可疑值,反之则保留,常取0.95的置信度。
如果测定数据较少,测定的精密度也不高,因Q与Qp,n值接近而对可疑值的取舍难以判断时,最好补测1~2次再进行检验就更有把握。
2)格鲁布斯法
①计算统计量G
G值=x疑-x平/S
说明可疑值对相对平均值的偏离较大,则以一定(0.90或0.95)的置信度弃去可疑值,反之则保留。在运用格鲁布斯法判断可疑值的取舍时,由于引入了t分布中最基本的两个参数x和s,故该方法的准确度较Q法高,因此得到普遍采用。
3)显著性检验
其实质是检验新方法有无系统误差,即检验新方法的平均值同已知的真值T或理论值之间有无显著差异。若有,就说明存在明显的系统误差;反之,纯属随机系统误差引起的。认为是正常的,从而对分析方法的准确度作出评价。
常用的有t检验法。先算出平均值和平均值的标准偏差,按下式计算t:
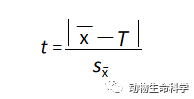
(5)盲法
2)双盲
双盲法是科学方法的重要组成部分,可防止研究成果中产生观察者偏差的影响。在医学、心理学、社会科学和鉴定学中,盲法研究是研究领域的重要工具。双盲实验被认为达到了较高水平的科学要求。
双盲实验中,无论是受试者还是研究人员都不知道对照组的治疗方法以及所属的实验组。只有在所有的数据被记录(以及在某些情况下分析后)研究人员才可能了解真相。例如,在卒中研究中,第一名研究人员对不同受试者分配了一系列代码;第二名研究人员被告知代码的意义,由于不知道实验的分组,所以不会影响整个研究。在这个体系下往往是动物的重量及动物的脑损伤程度得到更理想的分配。因此,双盲(或随机)测试成为首选,因为它一般能给予最准确的结果。无论在治疗或测量,双盲方法可以适用于任何实验情况。双盲法比较容易在药物研究中进行,制定的药物和对照(一个既定的药物或安慰剂)有可辨外观(颜色、味道等)。患者或动物随机分为对照或实验组,由研究协调员编码,药品也由研究协调员编码。患者或动物以及研究人员不知道哪些患者或动物正在接受哪种治疗或期望哪种结果,直到研究结束,代码被解密。
3)三盲法
(6)实验对照组类型
任何一个实验都是要验证(探究)实验变量和反应变量之间的因果关系。每一个实验都有实验目的,按照实验目的,找出实验中要研究的因素(指实验中由实验者控制的特定实验对象的因素)及相应的实验因素中的变量(指实验中由实验者控制的特定实验对象的因素的变量)。通常,一个实验总要进行对照实验(实验组和对照组)。用于对比的实验对象组一般称为对照组,对照实验(即对比实验)只是一个条件(即因素)不同,其他条件(因素)都相同的情况下所进行的一组实验,借此分析条件(因素)和结果之间的关系。在测试中,设置重复样品并同时拥有一个阳性对照和阴性对照是很好的做法。从重复样品得到的结果可以平均计算,如果一个样品的结果,与其他样品的结果不一致,必须通过特定的分析,来决定它是不是实验误差的结果,而被舍弃(程序错误、设备故障、记录错误或其他问题)
阳性对照从以往实验中总结出与实际治疗或程序非常类似的方法,并可以得到阳性结果。阴性对照通常得到阴性结果。阳性对照确保即使受试样品没有阳性结果,实验者也可以依据阳性结果判断实验本身的有效性。阴性对照确保在此条件下得到的结果并非是由测量不当而得到的阳性结果,通常阴性结果作为一个背景值从结果中减除。有时阳性对照以标准曲线形式出现。以往研究所得数据或参数可作为一个历史对照。历史对照来自不同实验,因而有不同的实验条件,它们通常是一种次要的对照形式。
如经常在实验室培训中使用的蛋白质含量测定。提供给学生的是一种含未知量的蛋白的液体样品。他们的工作是在一个对照实验中,确定这个样本中的蛋白质含量。演示实验中应提供已知蛋白质浓度的标准溶液。学生们应准备几种包含标准蛋白的不同稀释浓度的不同阳性对照样品(以获取一个标准曲线),阴性对照样品应包含蛋白分析的所有试剂但不含蛋白。在这个例子中所有样品应一式2份或3份。此分析法选用比色分析法,通过检测蛋白分子相互作用所形成的彩色复合物以及补充染料,利用分光光度计检测产物的吸光度。在这个例子中,未知样品中蛋白的浓度可以通过将样品吸光度和标准曲线进行比较进而确定。
体内研究与体外研究遵循相同的逻辑结构,所有的实验对照都通用,但这些实验对照情况是不同的。
实验组接受不同剂量的药物(至少有三个以上不同的剂量,以绘制一个剂量反应曲线)。剂量选择要根据药物的效力。如果选择正确的剂量,一次实验中可以包括具有完全效力的剂量,部分效力的剂量和无效剂量。
阳性对照是一种干预方法,比如一种药物、疗法或医疗器械,这种干预方法的有效性以前已经是明确的。阳性对照的目的是给出阳性结果并与实验组的结果进行程度上的比较。卒中研究阳性对照很好的例子就是右啡烷( dextrorphan)。右啡烷是一种非竞争性的N-甲基-D-天门冬氨酸(NMDA)受体通道阻断剂,已经被证实对局灶性脑缺血实验模型有神经保护作用。在研究右美沙芬是否对局灶性脑缺血实验模型有神经保护作用的实验中,同时设置右美沙芬和右啡烷两组,以右啡烷组为阳性对照,与右美沙芬组的结果进行程度上的比较,以证明右美沙芬( dextromethorphan)是否对局灶性脑缺血实验模型有神经保护作用。
在体内研究中,假手术对照组动物所进行程序与实验组动物类似,但并不参与疾病模型的关键步骤。例如,在远端卒中模型中,动物大脑有视窗,颈部有切口,但没有大脑中动脉和颈动脉栓塞。