上市3周年 | RWD激光散斑血流成像系统,服务全球100+用户,助力50+研究成果

从2002年启程,跨越20载,瑞沃德始终致力于创新,为生命品质的提升贡献智慧和力量。在活体成像研究领域,瑞沃德自主研发激光散斑血流成像系统,帮助科研工作者构建非侵入性脑血流监测研究体系。
RWD激光散斑血流成像系统RFLSI Ⅲ
自2019年上市以来,瑞沃德激光散斑血流成像系统装机量已突破100+台,获得如首都医科大学附属北京天坛医院、北京脑重大疾病研究院、斯坦福大学医学院、杜克大学医学中心等众多一流科研单位的青睐;并与全球 200 多家客户进行了线上演示和线下试用;助力科研人员在Gut、Blood、Diabetes、Theranostics、Nature Communications等专业期刊发表学术成果60多篇,为科研产出全面提速。
肠道微生物群是许多中风风险因素的重要因素。然而,中风和肠道菌群之间的双向相互作用在很大程度上仍然未知。
2021年2月,南方医科大学珠江医院尹恝、周宏伟、何彦研究团队在知名期刊《Gut》(2021 IF=23.059)发表了《Rapid gut dysbiosis induced by stroke exacerbates brain infarction in turn》一文。

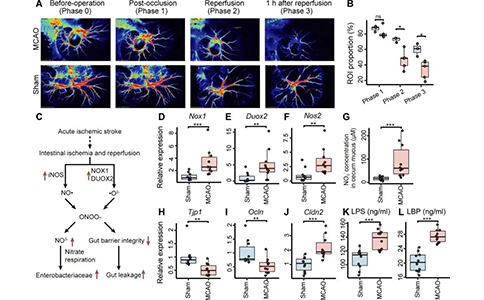
团队成员发现脑缺血迅速引起肠道缺血,并通过自由基反应产生过量硝酸盐,导致肠道菌群扩张失调。肠杆菌科富集通过增强全身炎症而加重脑梗死,是卒中患者主要不良预后的独立危险因素。使用氨基胍或超氧化物歧化酶减少硝酸盐生成或使用钨酸钠抑制硝酸盐呼吸均可抑制肠杆菌过度生长,减少全身炎症并减轻脑梗死。这些影响是肠道菌群依赖的,表明脑肠轴在中风治疗中的转化价值。这项研究揭示了中风和肠道失调之间的相互关系。缺血性中风会迅速引发肠道菌群失调,肠杆菌过度生长,进而加重脑梗死。
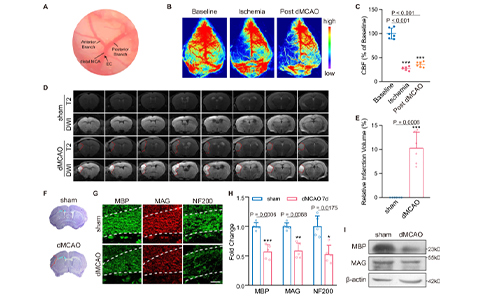
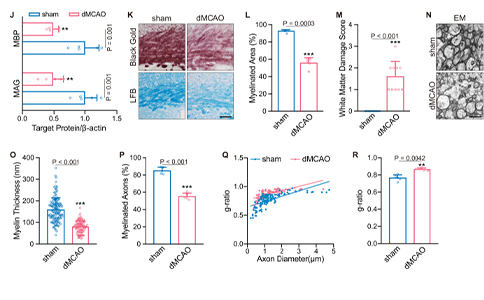
脑卒中后会出现远隔区继发性脑白质损伤,造成脑卒中患者远期预后不良。然而可能的机制尚不明确。国外学者在其他脑白质病变患者的研究中发现星形胶质细胞吞噬作用参与脱髓鞘损伤,吞噬髓鞘碎片后肿胀变形的星形胶质细胞能募集炎症细胞并参与脑白质病变。脂质运载蛋白2(Lipocalin-2,LCN2)作为反应性星形胶质细胞的重要标志物,其功能研究多集中于星形胶质细胞分泌后引发的炎性改变,而LCN2在继发性脑白质损伤及星形胶质细胞吞噬作用的相关研究仍不清楚。

2022年3月,南京大学神经病学研究所(南京大学附属金陵医院神经内科)团队在国际著名综合性期刊《Nature Communications》(2021 IF=14.919)在线发表文章《Astrocytic phagocytosis contributes to demyelination after focal cortical ischemia in mice》,发现急性局灶性脑皮质梗死后星形胶质细胞内源性LCN2表达升高,能与介导吞噬作用的受体LRP1结合,导致LRP1磷酸化,激活下游吞噬信号通路,造成星形胶质细胞吞噬活化,引起胼胝体髓鞘丢失。
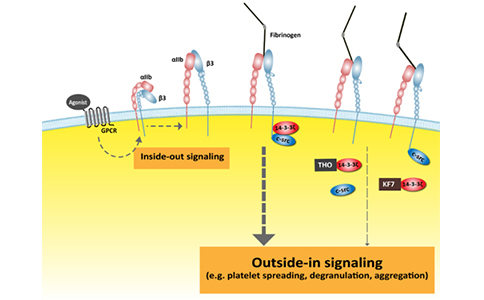
血小板是哺乳动物血液中主要的细胞成分之一,在血栓形成和止血过程中发挥关键作用。αIIbβ3整合素(αIIbβ3integrin)是血小板中特有的、与血小板激活密切相关的膜蛋白。临床中常使用的抗血栓药物依替巴肽、阿昔单抗和替罗非班,均是通过竞争性结合于αIIbβ3胞外域的配体结合区,通过抑制其与配体(如纤维蛋白原、纤维蛋白等)的结合发挥抗血栓作用,但这些药物会增加患者的出血风险。

下肢外周动脉疾病(PAD)是导致动脉粥样硬化性心血管疾病的第三大原因,为了促进缺血后血管的恢复,识别关键的内源性调节因子并探索增强其体内功能的途径是十分重要的。以往的研究表明,配体依赖的过氧化物酶体增殖物激活受体δ亚型(PPARδ)激活促进了血管生成。然而,低氧如何触发PPARδ及其在缺血后血管修复过程中的下游影响尚不清楚。

2022年3月,香港中文大学的研究者们在《Theranostics》(2021 IF=11.556)杂志上发表了“Endothelial PPARδ facilitates the post-ischemic vascular repair through interaction with HIF1α”的文章,该研究揭示了低氧诱导的内皮细胞PPARδ非依赖于配体的激活稳定了HIF1α,并且是HIF1α激活的关键调节因子,以促进缺血后血管内稳态的恢复。
在本研究中,研究者首先发现了内皮PPARδ的缺失延迟了组织的灌注恢复和修复,伴随着缺血后血管生成的延迟,损害了血管完整性的恢复,更多的血管渗漏和炎症反应增强。在分子水平上,缺氧上调和激活内皮细胞中的PPARδ,而PPARδ相互稳定HIF1α蛋白,以防止其泛素介导的降解。
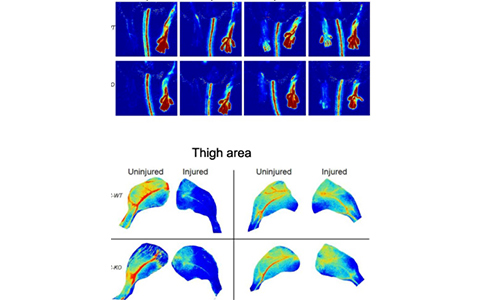
PPARδ直接与缺氧诱导因子1α(HIF1 α)的氧依赖降解结构域结合在PPARδ的配体依赖结构域上。重要的是,这种HIFα-PPARδ相互作用不依赖于PPARδ配体。腺相关病毒介导的稳定的HIF1α在体内的内皮靶向性过表达改善了小鼠后肢缺血后的灌注恢复,抑制了血管炎症,并增强了血管修复,以抵消PPARδ基因敲除的影响。













