港中文联合东南大学提出血管内靶向给药新策略
港中文联合东南大学提出血管内靶向给药新策略
微纳米机器人从内部或外部环境获取能量,从而实现主动运动。由于它们体积小,运动可控等特性使其能够广泛地应用于生物医学领域,尤其是血管内系统,如血栓清除、伤口愈合和药物输送。然而,实时跟踪这些机器人群一直是一项挑战,尤其是对于依赖于长时间暴露于电离辐射的成像模式。
本研究首先提出了一种控制与追踪策略,在该策略下,利用LSCI技术可以实现静态和动态血液环境中实时跟踪和导航微集群。该技术具有大成像视野、高时空分辨率和非侵入性等特点,通过分析灌注单元(PU),可以定量研究微群引起的动态对流变化,为研究微群行为及其与各种血液环境的相互作用提供了新方法。在该实验中,LSCI 通过对微集群和周围环境进行实时监测和成像,并对图像进行进一步分析,可实现在复杂的血管系统中对微集群的实时跟踪和导航。
研究者利用人体胎盘作为模型,进一步研究了在该策略下微集群在真实的组织环境中的成像和追踪结果。胎盘具有与人脑相似的软组织成分和复杂的血管结构,因此被认为是模拟真实血管环境并研究微集群定位与导航策略的理想模型。通过LSCI技术可以对具有分支结构的真实血管进行全视场成像,从而能够更有效地追踪微集群的位置。作者使用医用导管将纳米颗粒引入胎盘血管中,再利用旋转磁场控制纳米颗粒形成微集群,并测试微集群在顺流和逆流条件下在胎盘血管中的追踪和导航能力。结果显示,通过实时成像反馈和有效的控制策略,微集群在顺流和逆流条件下均能保持稳定,并显示出清晰的成像信号。研究者成功地对胎盘血管中的微集群进行连续五个周期的追踪和导航,总共导航距离约为400毫米。
上述结果表明,在LSCI的引导下,作者提出的控制与追踪策略能够在人体胎盘血管中实现相对长距离的微集群连续导航。研究为进一步实现微集群在真实组织环境中的应用提供了重要的基础。
接下来,研究者研究了在LSCI的引导下微集群在血管中的实时追踪和导航情况。结果显示,得益于有效的控制策略,在顺流和逆流导航过程中,微集群均能始终保持稳定和完整的状态,没有明显的颗粒损失。微集群在股静脉中展示出强烈的成像对比度,提高了导航的精度,并进一步实现了活体内的高效递送。定量研究结果表明,约85%的微集群能够在体内完成顺流和逆流导航后成功回收。这些结果证实了LSCI引导下的微集群在体内实时成像和导航的可行性,并为微纳米机器人集群在活体内高效递送的应用提供了有力的支持。
综上结果,LSCI引导下的磁性微集群可以在体外和体内血管环境中实现实时追踪和高精度导航。同时,该方法能够量化评估微集群与血液环境的相互作用,并在较高速血流条件下(平均流速55 mm/s)高效输送微集群。该研究为微纳米机器人集群在血液循环系统中实施主动靶向递送提供了有效的控制策略,并为基于微纳米机器人集群的治疗平台的开发和临床应用做出了贡献。
这项工作展示了磁性微集群在血管系统中的形成过程,以及其在LSCI引导下,在复杂血液环境中实时追踪和高精度导航微集群的能力。研究过程中分别在体内外血液环境应用纳米粒子构建出磁性微集群,通过高效的控制策略调控微集群的聚集行为,并采用LSCI技术进行实时追踪和导航。研究为实时追踪和导航微集群提供了一种有效的方法,展示出LSCI引导的微集群在血管系统中实施主动靶向递送的巨大应用潜力。
瑞沃德深耕生命科学研究领域21年,一直致力于为客户提供可信赖的解决方案和服务。在该研究中,研究人员使用了瑞沃德生产的激光散斑血流成像系统,为实验的顺利开展提供了支持。此外,瑞沃德还可提供该研究所涉及的动物手术造模、钙成像、电生理记录、免疫组化以及动物行为学等实验技术的完整解决方案。
近期,香港中文大学张立教授团队联合东南大学王乾乾教授团队,在Science Robotics 在线发表题为“Tracking and navigation of a microswarm under laser speckle contrast imaging for targeted delivery”的研究论文。博士生王庆龙与王乾乾教授为论文共同第一作者。研究报告了利用激光散斑对比血流成像技术(研究人员使用了瑞沃德生产的激光散斑血流成像系统)实时跟踪血管内的磁性纳米机器人集群并引导它们进行血管内导航的研究。研究结果展示了在激光散斑对比成像(LSCI)引导下对微集群在体内外复杂血液环境中进行高对比度成像和导航的潜力。这些发现为改进有针对性的血管内给药提供了机会。
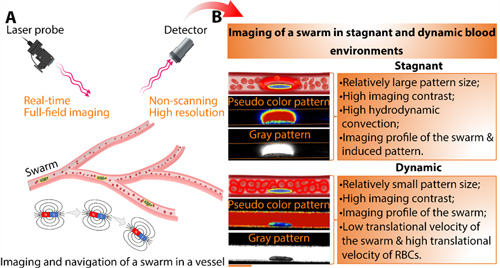
本研究首先提出了一种控制与追踪策略,在该策略下,利用LSCI技术可以实现静态和动态血液环境中实时跟踪和导航微集群。该技术具有大成像视野、高时空分辨率和非侵入性等特点,通过分析灌注单元(PU),可以定量研究微群引起的动态对流变化,为研究微群行为及其与各种血液环境的相互作用提供了新方法。在该实验中,LSCI 通过对微集群和周围环境进行实时监测和成像,并对图像进行进一步分析,可实现在复杂的血管系统中对微集群的实时跟踪和导航。
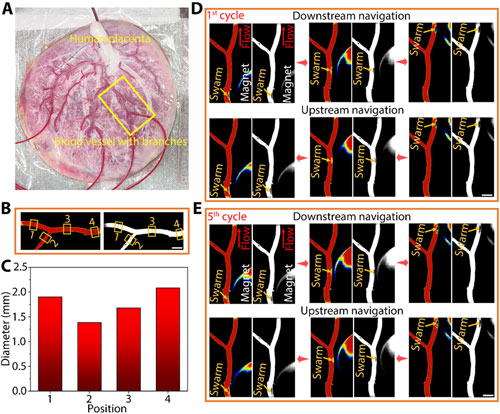
研究者利用人体胎盘作为模型,进一步研究了在该策略下微集群在真实的组织环境中的成像和追踪结果。胎盘具有与人脑相似的软组织成分和复杂的血管结构,因此被认为是模拟真实血管环境并研究微集群定位与导航策略的理想模型。通过LSCI技术可以对具有分支结构的真实血管进行全视场成像,从而能够更有效地追踪微集群的位置。作者使用医用导管将纳米颗粒引入胎盘血管中,再利用旋转磁场控制纳米颗粒形成微集群,并测试微集群在顺流和逆流条件下在胎盘血管中的追踪和导航能力。结果显示,通过实时成像反馈和有效的控制策略,微集群在顺流和逆流条件下均能保持稳定,并显示出清晰的成像信号。研究者成功地对胎盘血管中的微集群进行连续五个周期的追踪和导航,总共导航距离约为400毫米。
上述结果表明,在LSCI的引导下,作者提出的控制与追踪策略能够在人体胎盘血管中实现相对长距离的微集群连续导航。研究为进一步实现微集群在真实组织环境中的应用提供了重要的基础。
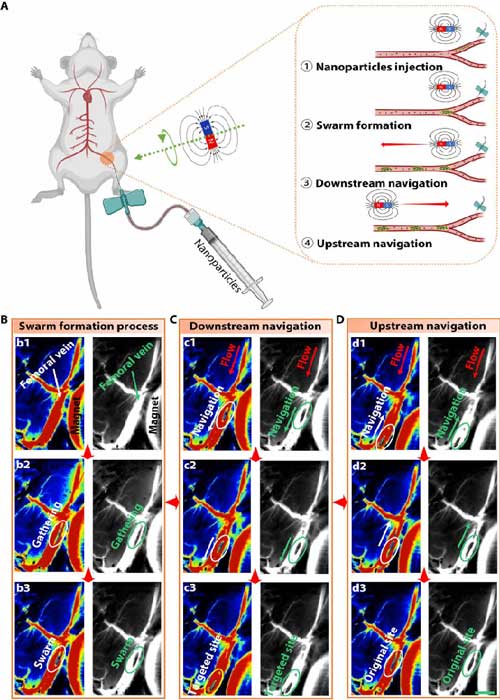
接下来,研究者研究了在LSCI的引导下微集群在血管中的实时追踪和导航情况。结果显示,得益于有效的控制策略,在顺流和逆流导航过程中,微集群均能始终保持稳定和完整的状态,没有明显的颗粒损失。微集群在股静脉中展示出强烈的成像对比度,提高了导航的精度,并进一步实现了活体内的高效递送。定量研究结果表明,约85%的微集群能够在体内完成顺流和逆流导航后成功回收。这些结果证实了LSCI引导下的微集群在体内实时成像和导航的可行性,并为微纳米机器人集群在活体内高效递送的应用提供了有力的支持。
综上结果,LSCI引导下的磁性微集群可以在体外和体内血管环境中实现实时追踪和高精度导航。同时,该方法能够量化评估微集群与血液环境的相互作用,并在较高速血流条件下(平均流速55 mm/s)高效输送微集群。该研究为微纳米机器人集群在血液循环系统中实施主动靶向递送提供了有效的控制策略,并为基于微纳米机器人集群的治疗平台的开发和临床应用做出了贡献。
研究方法亮点
这项工作展示了磁性微集群在血管系统中的形成过程,以及其在LSCI引导下,在复杂血液环境中实时追踪和高精度导航微集群的能力。研究过程中分别在体内外血液环境应用纳米粒子构建出磁性微集群,通过高效的控制策略调控微集群的聚集行为,并采用LSCI技术进行实时追踪和导航。研究为实时追踪和导航微集群提供了一种有效的方法,展示出LSCI引导的微集群在血管系统中实施主动靶向递送的巨大应用潜力。
瑞沃德深耕生命科学研究领域21年,一直致力于为客户提供可信赖的解决方案和服务。在该研究中,研究人员使用了瑞沃德生产的激光散斑血流成像系统,为实验的顺利开展提供了支持。此外,瑞沃德还可提供该研究所涉及的动物手术造模、钙成像、电生理记录、免疫组化以及动物行为学等实验技术的完整解决方案。
截止目前,瑞沃德产品及服务覆盖海内外 100 多个国家和地区,客户涵盖全球2300+医院,1000+科研院所,6000+高等院校,已助力全球科研人员发表SCI文章14500+,获得行业广泛认可。
如果您想免费试用瑞沃德RFSLI ZW激光散斑血流成像系统
点击填写申请
会有专业人员与您联系
相关推荐
评论列表共有 0 条评论
暂无评论
发表评论
取消回复













