暨南大学张力课题组发现运动抗焦虑的表观遗传学机制
生命在于运动。在现代社会,生活节奏快、工作压力大和娱乐时间少等因素导致焦虑、消极的情绪如野草般蔓生,抑郁症及焦虑症这一心理疾病在普通人群中越来越常见。尤其如今在新冠大流行期间,有数据显示,人们的体育活动平均减少了32%,同时,报告显示很少运动的他们感到更加沮丧、焦虑和孤独。进一步的心理健康调查分析显示,那些每天大部分时间是坐着的人,抑郁和焦虑感更为严重。繁重的工作之余去健身房跑跑步,不仅可以强身健体,也可以放松心情,提高免疫力。对普通人来说,有氧运动是推荐的运动形式,其主要方式为慢跑、快走、打太极拳等。大量的人群研究支持长期运动对情感和认知功能的改善,并能有效降低罹患精神疾病的风险。那么关于运动改善脑健康的机制研究,可以为我们的科学运动提供依据。
暨南大学粤港澳中枢神经再生研究院张力课题组,在苏国辉院士支持下,自2017年以来聚焦“运动与脑健康”这一重大科学问题,构建针对不同情感及认知障碍的运动干预范式,发现了慢性有氧运动介导神经可塑性改善的关键分子通路(Sci Adv 2019),解析了运动对皮层兴奋-抑制微环路重塑的神经机理(Mol Psychiatry 2021),初步阐释了运动改善突触和神经网络的分子细胞机制。近日,课题组在Advanced Science期刊发表题为“Physical exercise prevented stress-induced anxiety via improving brain RNA methylation”的论文,对运动介导的外周-中枢表观遗传学效应做了进一步诠释。
本研究首先建立了慢性束缚压力应激(CRS)小鼠模型,发现14天跑步机训练可以有效预防焦虑样表型发生。对前额叶皮质(PFC)进行基于N6-甲基腺苷(m6A)修饰的转录组学测序,可见运动能有效恢复CRS后降低的脑内m6A水平,且这些差异表达的m6A位点多数位于兴奋性突触相关基因的转录本上(图1)。而通过特异性过表达及敲低病毒进行人为操纵RNA去甲基酶ALKBH5的表达水平,证实了运动预防焦虑样表型发生,依赖于其对脑内m6A水平的改善(图2)
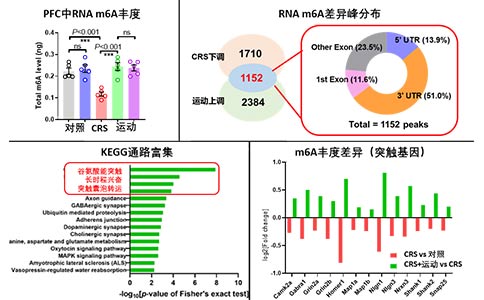
图1 有氧运动调控CRS小鼠脑内RNAm6A模式
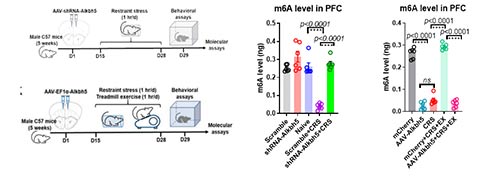
图2 人为操纵RNA去甲基酶ALKBH5的表达水平,证实运动预防焦虑样表型发生
通过进一步的探究对运动改变脑内RNA m6A的生物学机制进行了解析。RNA m6A修饰主要依赖于包括S-腺苷-甲硫氨酸(SAM)在内的甲基化供体;该课题组研究发现在有氧运动小鼠中,血清和脑内的SAM水平显著上升;而对不同外周器官进行比较,发现肝脏中的SAM合成酶(Mat1a)的表达明显提高;进一步通过特异性敲低肝脏中Mat1a基因表达,证实了运动改善脑内RNA m6A及抗焦虑的作用依赖于肝脏内SAM的生物合成(图3)。
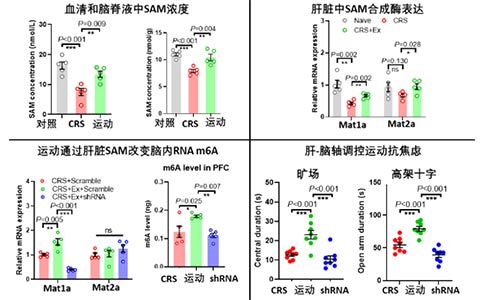
图3 长期运动通过肝-脑轴介导RNA m6A改变和抗焦虑效应
该研究主要发现,慢性有氧运动通过促进肝脏中氨基酸代谢,分泌特定的甲基化供体(S-腺苷-甲硫氨酸)进入脑,在前额叶皮质mPFC区域介导兴奋突触相关转录本的RNA甲基化(m6A),改善皮层神经网络,增强小鼠对慢性束缚环境压力的抵抗,防止焦虑样行为的发生。
综上所述,这篇论文的研究成果,为解释运动的脑健康效果提供了一个新的视角;而从代谢-表观遗传-神经网络这个角度来诠释运动和健康的机制,为我们更好评估运动疗效、科学运动提供了理论依据。所以,为了迎接更健康的明天,一起跑起来吧!
论文全文链接:
https://doi.org/10.1002/advs.202105731













