唐氏综合征相关基因USP25调控阿尔茨海默病理新机制
文章概述
唐氏综合征(Down syndrome, DS),又称21三体综合征,是一种最常见的智力障碍疾病。已有的研究表明,DS是早发性阿尔茨海默病(Alzheimer’s disease, AD)的重要危险因素之一,几乎所有的DS患者在40岁时都表现出AD神经病理,大约2/3的DS患者在60岁时出现AD症状。21号染色体编码的基因在AD发病机制中起着关键作用,包括引起淀粉样蛋白前体(Amyloid Precursor Protein, APP)的基因拷贝数增加、促进病理性淀粉样蛋白生成等。21号染色体上的泛素特异性蛋白酶USP25的基因能够调节AD中小胶质细胞稳态,但是,USP25是否会影响淀粉样蛋白的病理过程目前仍不清楚。2022年3月1日,厦门大学以及温州医科大学的研究团队在《The Journal of Clinical Investigation》期刊上发表题为“USP25 inhibition ameliorates Alzheimer’s pathology through the regulation of APP processing and Aβ generation”的研究论文,该文章证实,USP25可通过减少APP和BACE1(APP剪切酶)的泛素化以及溶酶体降解,促进了APP的剪切以及Aβ的生成。该研究的结果揭示了从DS发展到AD的关键机制,同时提供了一种潜在的改善AD病理的新策略。

核心观点
1、21号染色体三体加重了5×FAD小鼠(一种AD小鼠模型)大脑中的淀粉样蛋白病变;
2、过表达USP25增加了5×FAD小鼠脑内淀粉样蛋白沉积,而USP25基因缺失则减少了小鼠脑内淀粉样蛋白沉积;
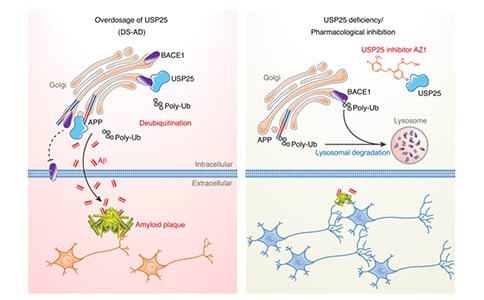
3、USP25通过减少APP和BACE1的泛素化以及溶酶体降解,从而促进APP的切割和Aβ的生成;
4、利用药理学手段抑制USP25可以改善5×FAD小鼠大脑中淀粉样蛋白病理。
研究结果分析
1. USP25基因拷贝数增加可加重AD小鼠淀粉样蛋白的病理改变
为了研究21号染色体三体是否影响了AD的病理,研究者通过利用5×FAD 小鼠和Dp16 小鼠(一种DS小鼠模型)进行杂交,形成了一种DS-AD联合小鼠模型。利用免疫印迹分析证实,与5×FAD 小鼠相比,DS-AD小鼠皮质中USP25、APP和APP-羧基末端片段(APP- CTFs)的表达明显上调。组织免疫荧光结果显示,在5月龄的DS-AD小鼠海马中,病理性的淀粉样斑块沉积更加显著。考虑到USP25 基因位于21号染色体上,为了确定USP25是否影响DS-AD背景下的淀粉样蛋白病理,研究者5×FAD小鼠与BAC-Tg-USP25小鼠(USP25过表达小鼠)杂交。组织免疫荧光结果显示,在6月龄的5×FAD:BAC-Tg-USP25小鼠海马中,其病理性淀粉样蛋白斑块数量较5×FAD小鼠显著增加,这表明将USP25基因本身拷贝数上调就足以加重AD小鼠的Aβ的病理。

2. Usp25基因缺陷可缓解AD小鼠淀粉样蛋白病理
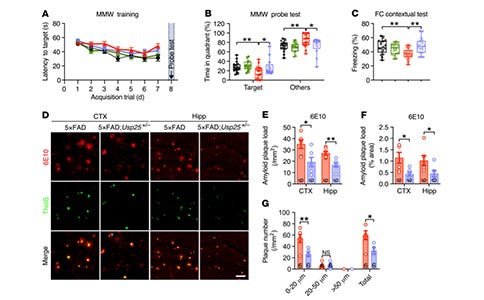
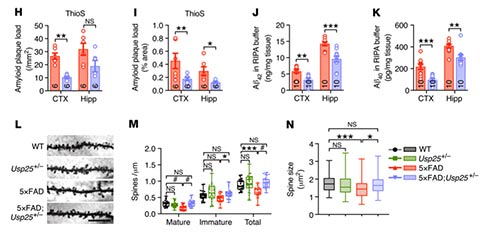
与同窝野生型(Wild Type, WT)小鼠相比,Usp25 -/-小鼠没有表现出体重和认知行为异常。但是,对于Usp25基因缺陷是否会影响淀粉样病变仍是未知的。通过将Usp25+/-小鼠与5×FAD小鼠杂交,产生了5×FAD:Usp25+/-小鼠。研究者评估了5×FAD:Usp25+/-小鼠的学习记忆能力,发现Usp25基因缺陷改善了AD小鼠在水迷宫测试和条件恐惧测试中的认知表现。随后,研究者检测了AD小鼠淀粉样蛋白斑块沉积情况,与5×FAD 小鼠相比,6月龄的5×FAD:Usp25+/-小鼠皮质和海马中淀粉样蛋白斑块沉积减少;并且通过ELISA检测到,AD小鼠Usp25下调能够显著降低皮层和海马中可溶性Aβ40和Aβ42的水平。此外,高尔基染色结果显示,5×FAD小鼠皮质中树突棘存在缺陷,而5×FAD:Usp25+/-小鼠中得到恢复。这些结果表明,Usp25表达下调能够缓解5×FAD小鼠的淀粉样蛋白病理和突触缺陷。
3. USP25能够调节淀粉样蛋白APP的加工过程
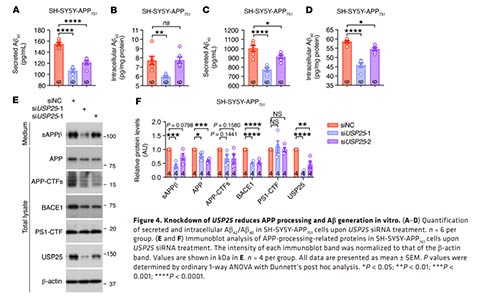
Aβ的产生源于β和γ分泌酶对跨膜前体APP的剪切。为了确定USP25下调引起的淀粉样蛋白沉积的减少是否源于APP加工过程的改变,研究者通过免疫印迹分析对APP加工通路中各种蛋白表达进行了表征。结果显示,Usp25缺乏降低了6月龄5×FAD:Usp25+/-小鼠皮质中APP及其剪切产物(α-和β- CTFs)的水平;而过表达USP25显著增加了6月龄BAC- Tg-USP25小鼠皮质中APP和BACE1的表达。
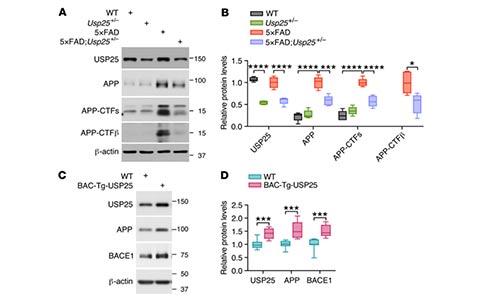
与在体实验结果一致,在人源过表达APP的SH-SY5Y-APP751细胞中,敲除USP25能够显著减少细胞内Aβ40和Aβ42的分泌。此外,敲除USP25能够减少APP、APP-CTFs、sAPPβ、BACE1的表达。另外,在APP过表达HEK293T细胞中过表达USP25能提高APP蛋白水平。抑制溶酶体降解能够废除过表达USP25所引起APP的改变。并且过表达USP25还会导致BACE1的表达增加,而过表达泛素则会降低BACE1表达水平,这表明USP25通过BACE1的泛素化来调控BACE1的表达。这些结果表明,USP25通过上调淀粉样蛋白加工通路的各种成分,如APP和BACE1,来增加Aβ的积累。
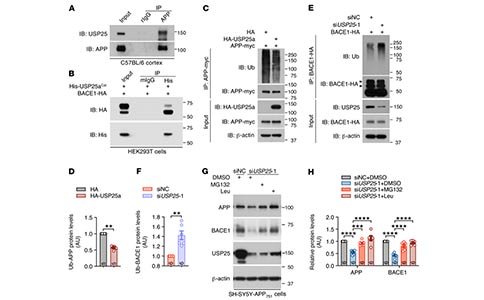
4. USP25促进BACE1的去泛素化和APPβ的剪切
为了确定USP25调控APP加工和Aβ生成的潜在分子机制,研究者进一步验证了USP25与APP以及BACE1之间的相互作用。USP25过表达减少了APP多聚泛素化的数量,而USP25敲除增加了BACE1多聚泛素化的水平。并且通过耗竭USP25介导的APP和BACE1降解可被抑制蛋白酶体和溶酶体降解途径所逆转。
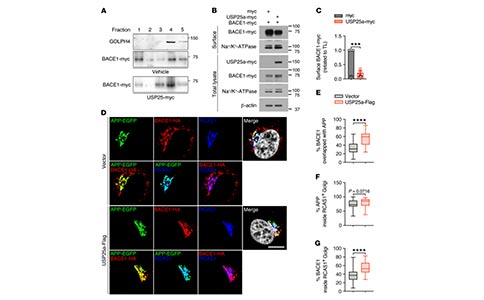
此外,研究者利用梯度蔗糖进行了亚细胞分离,发现USP25过表达增加了BACE1在高尔基体中的积累。为了进一步证实USP25对BACE1转运的影响,研究者利用质膜分离实验,观察到USP25过表达显著减少了细胞表面BACE1的分布,进一步的免疫染色分析显示,过表达USP25后,BACE1进入RCAS1阳性高尔基体比例增加,BACE1与APP共定位的比例增加。这些研究结果表明APP和BACE1是USP25底物,这些成分的转运/加工可以通过USP25介导的去泛素作用来调控。
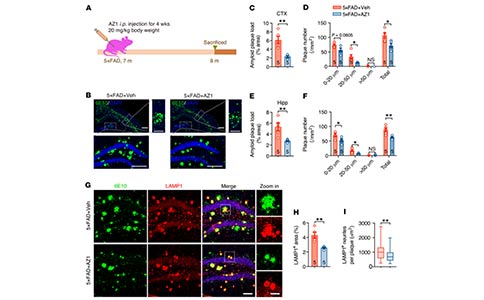
5. 抑制USP25可改善AD小鼠的淀粉样病变
研究者利用重组的USP25体外催化系统找到了一个可以强力抑制USP25酶活性的化合物AZ1。进一步的免疫印迹分析证实,AZ1能够显著降低了5×FAD小鼠皮质中APP和APP- CTFs的含量。为了评价抑制USP25对体内淀粉样蛋白沉积的作用,研究者在5×FAD小鼠腹腔连续注射USP25抑制剂AZ1(20 mg/kg/d,28天)。随后,通过组织学分析,观察到注射AZ1的5×FAD小鼠大脑中淀粉样蛋白斑块的数量有所减少。并且,AZ1也会减少LAMP1和ATG9A表达阳性的营养不良神经突的数目。这些结果表明,通过药物抑制USP25活性可以改善AD小鼠模型中淀粉样蛋白的负荷。
6. USP25的表达与AD患者大脑病理变化相关
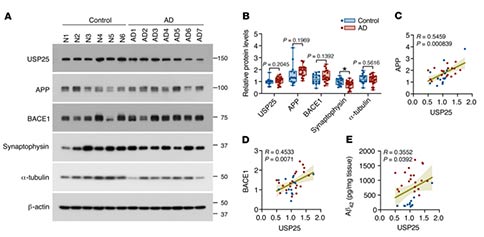
研究者进一步利用AD患者和年龄相匹配的对照组的临床尸检样本比较了大脑中USP25表达水平,偶发性AD患者大脑中USP25蛋白的水平与对照组并无差别;然而利用Spearman相关分析发现,AD患者皮质中USP25和APP、BACE1以及Aβ42之间的量存在正相关。提示USP25介导的淀粉样蛋白通路在AD发病机制中的潜在作用。
总结
亮点研究方法