调节小胶质细胞,有望作为预防和限制血管性认知损伤进展的途径
2021年中国卒中学会第七届学术年会上有数据表明,全球患脑小血管疾病(cSVD)人数高达7.5亿,其中中国约有1-2亿人。随着全球老龄化的加剧,脑小血管疾病(cSVD)作为随年龄增长而高发的小血管病,将会对中老年人乃至社会造成广泛影响。
高血压是引发cSVD的危险因素,其他因素还包括年龄、卒中、遗传等。同时,cSVD也是导致血管性认知障碍(VCI)的主要原因之一。
虽然对人类健康有着深远的影响,但是由于对cSVD的病理机制了解有限,国内外医学界目前仍没有针对cSVD的特定治疗方法。所以,现阶段对cSVD病理的研究,为下一阶段扩宽临床诊疗的思路起着决定性的作用。
相关研究表明,血脑屏障(BBB)功能障碍在cSVD的病理中起着关键作用。血脑屏障通透性的增加可导致小胶质细胞的持续激活,并诱导病理进展,特别是白质损伤。在健康条件下,血脑屏障以一种良好的调节方式发挥作用,以确保营养的提供,同时通过形成物理屏障保护脑细胞免受血液成分的伤害。MRI研究表明,cSVD患者血脑屏障通透性更高,血浆成分泄漏到实质将引起局部炎症反应,其中包括Fc受体诱导的小胶质细胞活化。
因此,深入了解血脑屏障与小胶质细胞的相互作用,有助于理解cSVD的病理。
血脑屏障与小胶质细胞新发现
2020年,在Top期刊Theranostics发表研究论文表明,消耗血脑屏障内促炎小胶质细胞,可以防止Ang II诱导的高血压小鼠的短期记忆损伤。

▲图1:Pharmacological depletion of microglia and perivascular macrophages prevents Vascular Cognitive Impairment in Ang II-induced hypertension 研究论文
这一新的发现支持大脑免疫细胞在高血压相关认知障碍发病机制中的关键作用,适当调节小胶质细胞密度和表型可能有望作为预防和限制血管性认知损伤进展的途径。
小胶质细胞是脑内的髓系细胞,其整个生命周期的维持依赖于自身的自我更新能力,由生长因子集落刺激因子1 (CSF1)及其受体(CSF1R)调控。早些时候的研究也发现了在长期Ang II输注模型中,激活的小胶质细胞与血脑屏障渗漏和短期记忆损伤密切相关。
该篇文献使用CSF1R酪氨酸激酶抑制剂(PLX5622)消除小胶质细胞,解读小胶质细胞对高血压诱导的认知损伤的关联性。
首先,作者对3个月大的雄性小鼠分含有PLX5622食物或正常喂养两组对照,同时所有小鼠皮下植入缓释泵用于Ang II(1µg/kg/min皮下注射)或生理盐水连续输注12周构建高血压模型,该模型呈现了与cSVD相关的病理特征,并进行后续行为学及病理等实验。
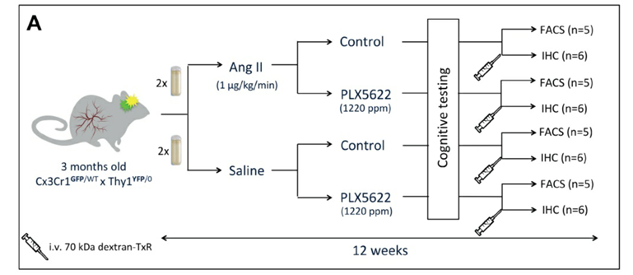
▲图2:小鼠实验
作者通过实验观察到,PLX5622能够消耗小胶质细胞,减少血管周围巨噬细胞和循环免疫细胞的数量。
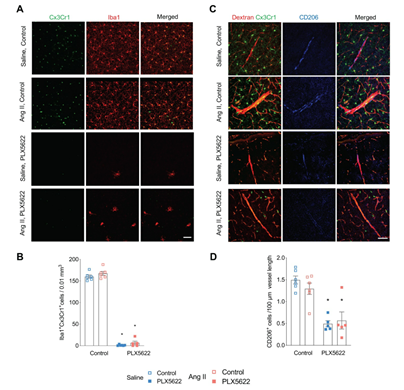
▲图3:PLX5622对小胶质细胞和血管周围巨噬细胞密度的影响
作者进一步发现,CD68标记的促炎小胶质细胞在血脑屏障渗漏处的数量增加了,并且被PLX5622成功消耗。
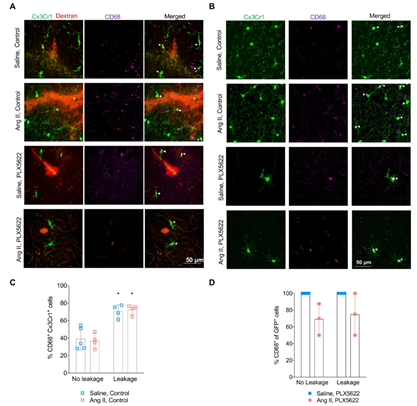
▲图4:小胶质细胞在血脑屏障泄漏中获得促炎表型,并被PLX5622消耗
接下来作者通过70kDa -葡聚糖探针(TxR)和血浆IgG蛋白渗入脑实质的情况来评估血脑屏障的通透性,实验表明PLX5622处理没有明显改善由于AngII引起的血脑屏障通透性的改变。
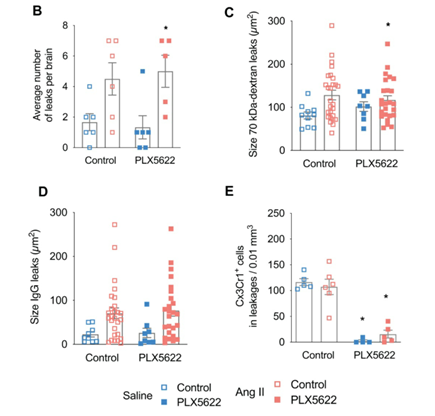
▲图5:PLX5622不能改善高血压引起的血脑屏障通透性改变
最后,作者通过Morris水迷宫(A,B,C)以及物体定位任务(D,E)分别评估长期记忆和短期记忆。结果显示小鼠的长期记忆表现不受Ang II和/或PLX5622治疗的影响。而Ang II型高血压小鼠短期记忆功能明显受损,经过PLX5622处理对Ang II型高血压小鼠有部分抑制作用。
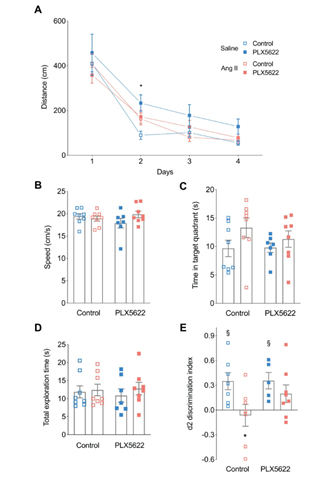
▲图6:Morris水迷宫评和物体定位任务评估长、短记忆
这项研究发现使用CSF1R抑制剂PLX5622消耗小胶质细胞时,可部分预防由于长时间输注Ang II引起的短期记忆损伤,而PLX5622对于认知的改善与血脑屏障通透性的变化无关。这是CSF1R治疗学发展的重要一步,同时作者指出需要进一步的研究来开发一种治疗方案,达到患者在短时间内小胶质细胞实现快速且安全消减的目的。

(▲植入式缓释泵)
皮下植入缓释泵是可靠的长期准确控制血药浓度稳定的给药方法,现在已经成为国际上比较公认药物造模的流行给药方式。
- 从小鼠到大鼠、家兔、狗、猪、猴等动物,均可以通过缓释泵装载药物升高血压。
- 操作简便,⼀次埋置操作,即可实现最⻓4周持续给药
- 给药速率稳定,保证每日给药量⼀致
- 泵体体积小,极大减少对动物自由活动的影响
- 减少反复抓取与注射给小鼠带来应激刺激,保证动物处于正常⽣理状态