心脏骤停复苏动物模型下脑神经功能,非折叠蛋白分支XBP1s的效应研究
心脏骤停和复苏动物模型的建立
1、用5%异氟烷诱导麻醉3-4个月龄小鼠,气管插管后,小鼠在进行CA前维持1.5%-1.7%的异氟烷吸入。
2、通过探头持续测量直肠温度,整个过程保持在36.5±0.5℃环境下。分别将电极针插入双侧前肢和左后肢,连续记录心电情况。
3、剃光颈部毛发,切开1cm皮肤切口,暴露出颈静脉。待生理状态稳定后,从颈静脉取血0.3 mL,随后从颈静脉注入0.5 mol/L KCl 30 μL诱发心脏停搏,以心电图波形监测CA的发生。
4、当CA发生后,停止肺通气。于CA后3分钟重新输注血液。CA后8分钟,将吸入的氧气调整至100%。CA 8.5分钟后,恢复机械通气,快速静推肾上腺素100 μL (32 μg/mL),然后持续输注肾上腺素20 μL/min。
5、单指按压胸部,每次按压约300次/分钟,直到恢复自发血液循环,即出现稳定的心电图窦性节律,此时肾上腺素输注随即停止,肾上腺素最大输注量应限制在300 µl。
6、如果在3分钟内不能恢复自发性血液循环,则放弃复苏,并将该动物排除在研究之外。一旦小鼠获得自主呼吸,就可以将其被从手术台上取出,至于温暖环境下恢复。
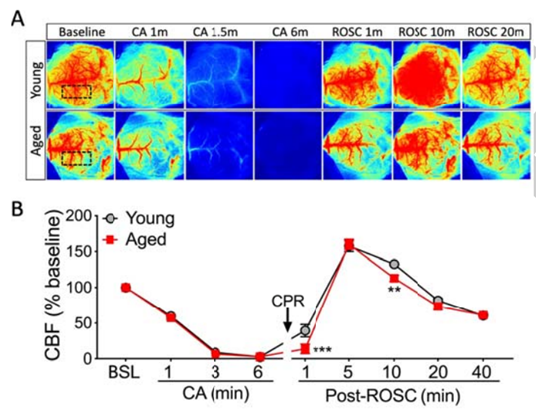
A不同年龄小鼠大脑皮层血流随心脏骤停-恢复的变化情况彩图
B不同年龄小鼠大脑皮层血流量随心脏骤停-恢复的变化情况量化数据
Abbr.CA- cardiac arrest;ROSC -Return of spontaneous circulation;CBF-cerebral blood flow
RFLSI Ⅲ 激光散斑血流成像系统
激光散班血流成像,助力心脏骤停复苏模型的脑血流研究。
非折叠蛋白分支XBP1s的效应研究
心脏骤停和复苏导致脑缺血再灌注(I/R)损伤,与脑神经元的死亡密切相关。为此,研究者们1通过促进受损的细胞功能的恢复,试图维持细胞内稳态,以此来开拓一种内源性的治疗方法。
非折叠蛋白反应(unfolded protein response, UPR)是一种提高细胞存活的通路,在内质网(ER)受损或内质网应激发生后,UPR将会被激活,其主要作用是恢复内质网稳态,促进细胞存活。
缺血性卒中或CA/复苏导致的脑I/R损伤会导致内质网应激并诱发UPR的激活。作为UPR的一个分支,转录因子XBP1的功能是上调葡萄糖代谢相关酶的表达,并且促进O-linked β-n-乙酰氨基葡萄糖(β-N-acetylglucosamine)的修饰,即O-GlcNAc糖基化。
具体实验方法就是通过基因导入和基因敲除技术获得Xbp1过表达和Xbp1缺失的两种小鼠。通过上述步骤建立小鼠心脏骤停和复苏动物模型,再进行行为学评估(Rotarod;Open field)和Neurologic score评分。
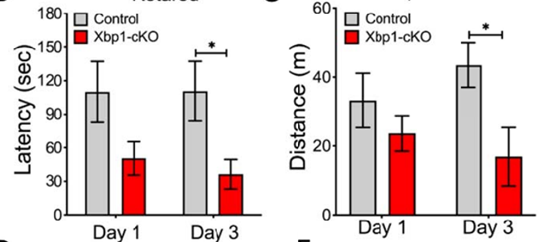
Latency:使用转棒仪,通过3次试验的平均数据计算从转棒上跌落的潜伏时间。每只小鼠在CA前连续3天接受旋转训练。
Distance:旷场实验,测算小鼠的活动距离
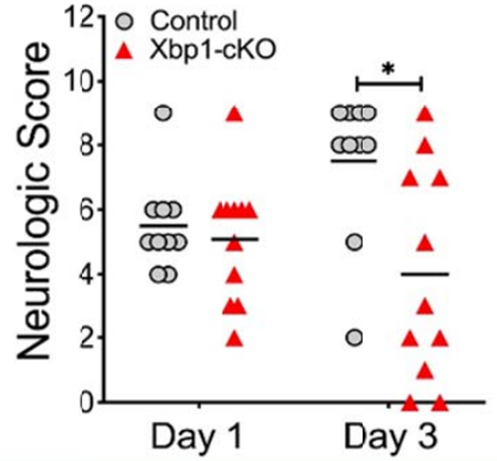
Neurologic score:用9分制评分表评估神经功能缺陷。(9分=正常,0分=严重伤害)
可以看出神经元特异性Xbp1敲除小鼠的CA行为学结果较差,而神经元特异性表达Xbp1的小鼠的CA行为学结果较好。实验结论:激活的XBP1可以对CA后的脑神经起到保护的作用。













